- FDA 임상 3상 승인…미국 협력사 통해 임상 실시

HK이노엔의 협력사인 브레인트리래보라토리스는 최근 미국 식품의약국(FDA)으로부터 테고프라잔의 임상 3상 시험계획(IND)을 승인받은 후 임상을 시작했다.
이번 임상은 미란성 위식도역류질환의 치료와 치료효과 유지를 살펴보는 방식으로 진행된다. 또한, 비미란성 위식도역류질환에 대해 테고프라잔과 프로톤펌프저해제(PPI) 계열 간 유효성과 안전성을 비교하는 시험도 진행한다.
HK이노엔은 지난해 12월 미국과 캐나다에 케이캡을 기술 이전했다. 올해 4월에는 미국 임상 1상 결과를 발표했다. HK이노엔 관계자는 “임상 2상을 생략하고 바로 임상 3상에 진입하게 됐다”며 “임상 1상을 디자인할 때 임상 2상에서 요구하는 조건도 충족할 수 있도록 했다”고 설명했다.
미국의 위식도역류질환 치료제 시장은 지난해 기준 약 4조원으로, 규모가 가장 크다. 미국의 첫 번째 칼륨경쟁적위산분비억제제(P-CAB) 계열 제품은 패썸의보퀘즈나(성분명 보노프라잔)가 있다. 보퀘즈나는 지난 5월 헬리코박터파일로리 제균을 위한 항생제 병용요법을 적응증으로 허가받았다.
곽달원HK이노엔 대표는 “케이캡의 글로벌 진출 속도가 더욱 빨라지고 있다”며 “이번 미국 임상은 글로벌 100개 국가 진출이라는 목표 달성에도 긍정적인 신호”라고 했다. 케이캡이 국내에서 개발된 P-CAB 계열 위식도역류질환 치료제 중 미국에 가장 먼저 출시될 것이라는 기대도 내비쳤다.
케이캡은 국내에서 정제 및 구강붕해제로 출시됐다. 미란성 위식도역류질환과 비미란성 위식도역류질환, 위궤양, 헬리코박터파일로리 제균을 위한 항생제 병용요법, 미란성 위식도역류질환 치료 후 유지요법 등 5개의 적응증을 보유하고 있다.
선모은 기자 suns@edaily.co.kr
ⓒ이코노미스트(https://economist.co.kr) '내일을 위한 경제뉴스 이코노미스트' 무단 전재 및 재배포 금지
많이 본 뉴스
많이 본 뉴스
MAGAZINE
MAGAZINE
Klout
Klout
섹션 하이라이트
섹션 하이라이트
브랜드 미디어
브랜드 미디어
- 모아보기
- 일간스포츠
- 이데일리
- 마켓in
- 팜이데일리









![“늘 마지막이라고 생각”… 예예, 미워할 수 없는 ‘킹’ 유발자 [IS인터뷰]](https://image.isplus.com/data/isp/image/2025/03/11/isp20250311000307.400.0.jpg)
![인터스텔라 한 편 뚝딱... 집에서 보는 ‘실감나는 우주’ [김지혜의 ★튜브]](https://image.isplus.com/data/isp/image/2025/03/16/isp20250316000120.400.0.jpg)
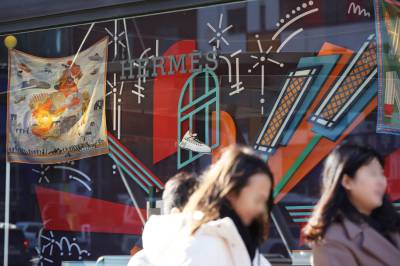






![[알림] 제3회 IS 스포츠 마케팅 써밋 아카데미 23일 개강](https://image.isplus.com/data/isp/image/2025/04/17/isp20250417000481.168x108.0.png)
![김종민·에일리·심현섭, 오늘(20일) 결혼… 연예인 하객들 바쁘겠네 [왓IS]](https://image.isplus.com/data/isp/image/2025/04/20/isp20250420000006.168x108.0.jpg)
![“1만원대 맞아?” BBQ 치킨에 짬뽕 무한리필 끝판왕 뷔페[먹어보고서]](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/04/PS25042000138B.jpg)


![한화에어로 유증 여전히 물음표…또 제동 걸렸다[위클리IB]](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/04/PS25041900219B.jpg)

![[VC’s Pick]류중희 전 퓨처플레이 대표 설립 ‘리얼월드’… 210억 투자 유치](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/04/PS25041900114T.jpg)

!['먹는 콜라겐 누적 매출 1조 돌파'…R&D·브랜딩 강점[뉴트리 대해부②]](https://image.edaily.co.kr/images/Photo/files/NP/S/2025/04/PS25041800445T.jpg)

당신이 좋아할 만한 기사
브랜드 미디어
브랜드 미디어
유재석, 미담 또 있다… 임우일 사고 수습 위해 사비로 전부 구매
대한민국 스포츠·연예의 살아있는 역사 일간스포츠일간스포츠
이데일리
이데일리
윤여정, 아들 커밍아웃 고백 “뉴욕에서 결혼… 사위를 더 사랑해”
대한민국 스포츠·연예의 살아있는 역사 일간스포츠일간스포츠
일간스포츠
일간스포츠
“1만원대 맞아?” BBQ 치킨에 짬뽕 무한리필 끝판왕 뷔페[먹어보고서]
세상을 올바르게,세상을 따뜻하게이데일리
이데일리
이데일리
한화에어로 유증 여전히 물음표…또 제동 걸렸다[위클리IB]
성공 투자의 동반자마켓인
마켓인
마켓인
국내 TPD 회사는 저평가 되었나…당면한 숙제는 '임상'
바이오 성공 투자, 1%를 위한 길라잡이팜이데일리
팜이데일리
팜이데일리