- (Free MP3) 모기 이용해 말라리아 잡는다
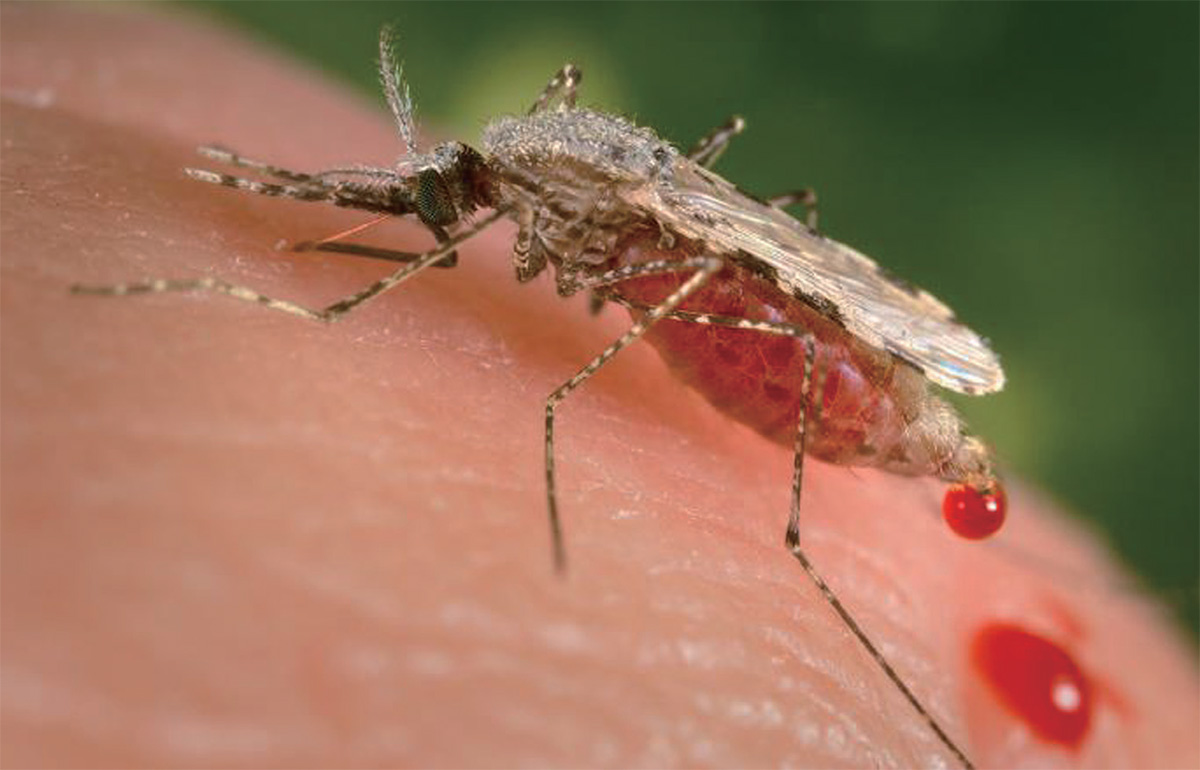
HUMANS BITE BACK
Scientists have genetically modified mosquitoes to be malaria-resistant.Malaria will strike more than 200 million people this year, according to the World Health Organization, and will kill nearly half a million. Although the disease can be treated, in some parts of the world—sub-Saharan Africa, in particular—the medicines needed are often unavailable. And worse, the parasite that causes malaria is becoming more and more resistant to the drugs we have to fight it.
That’s why several research groups are working on genetic modifications to mosquitoes that would prevent them from spreading the parasite. The latest advance comes from the University of California, Irvine, which has created a mosquito that not only doesn’t transmit malaria but also passes on this trait to 99.5 percent of its offspring.
That’s quite an achievement, since many traits inherited in a more typical fashion go to only a fraction of an organism’s offspring, says researcher Anthony James. His team used a gene-editing technique called CRISPR to insert two genes into the insect’s genome to confer malarial resistance. Given the high rate of inheritability, the resistance would theoretically spread quickly throughout a population once it has been introduced, James says.
The UC Irvine team worked on the genome of Anopheles stephensi mosquitoes, which are a main vector of malaria in India, where there are more than 1 million cases annually and more than 500 deaths. There’s reason to believe the technique would work in other species as well, according to a study describing the finding, published November 23 in the journal Proceedings of the National Academy of Sciences. David O’Brochta, a researcher at the University of Maryland who wasn’t involved in the study, says “this kind of system could help defeat malaria.”
In the past couple of years, CRISPR has changed the way much genetic modification is done. It works by allowing scientists to cut DNA at a specific location in the genome, and to insert desired genes. Compared with previous methods, it is much quicker and cheaper. This technique of introducing malaria resistance used by the UC Irvine team was, for example, first demonstrated in fruit flies earlier this year; just a few months later, the team successfully applied the same method to mosquitos. Older gene-editing techniques would have taken much longer to fine-tune for different animals.
The two genes James’s team has introduced are modified mouse immune genes, which bind to the malaria parasites and prevent them from recognizing their host and moving around in the mosquito’s body. “You can think of it as [being] blinded,” James says. As a result, the parasite cannot get into the animal’s salivary gland and, therefore, doesn’t make it into humans when the mosquitoes bite.
James says the innovation needs to be tweaked slightly before being applied in the field, and introducing genetically modified organisms into the wild would require regulatory approval from foreign countries where malaria is endemic. But he’s hopeful it could be introduced sometime in the next several years.
In the short time it has been in use, CRISPR has raised a number of ethical questions. In April, scientists used the technique to modify human embryos; the team attempted to avoid ruffling feathers by using nonviable embryos, but the experiment created a firestorm of controversy anyway. James says more research needs to be done on likely long-term effects of the modification before using it in the real world. There is some concern, for example, about what might happen if the “gene drive”—the genetic mechanism that causes the trait to be passed on to nearly all offspring—were to make its way into another organism, O’Brochta says; perhaps an undesirable gene might spread through a whole population of animals, wiping out a species. But this seems unlikely, James says, and at this point the potential benefits of helping to stop malaria appear to outweigh the risks.
모기 이용해 말라리아 잡는다
‘유전자 가위’로 말라리아 내성 유전자를 모기에 삽입하고 자손에게 물려주는 비율 크게 높여세계보건기구(WHO)에 따르면 올해 2억 명 이상이 말라리아에 걸려 약 50만 명이 목숨을 잃을 수 있다. 치료할 수 있는 병이지만 세계 일부 지역, 특히 아프리카 사하라 사막 이남 지역에선 필요한 약이 공급되지 않는 경우가 적지 않기 때문이다. 설상가상으로 인간이 보유한 약에 말라리아 원충의 내성이 갈수록 커지고 있다.
모기의 유전자를 변형해 원충을 퍼뜨리지 못하도록 하는 방법을 여러 단체가 연구하는 이유다. 최근 캘리포니아대학(UC 어바인)에서 진일보한 방법이 발견됐다. 말라리아를 퍼뜨리지 않을 뿐 아니라 후대의 99.5%에게 이 같은 특성을 물려주는 모기가 개발됐다.
그것은 대단한 성과다. 더 전통적인 방식으로 유전되는 대다수 특질은 한 생명체의 자손 중 극히 일부에게만 전달된다고 앤서니 제임스 연구원은 말한다. 그의 연구팀은 모기 유전체에 2개의 유전자를 삽입해 말라리아 내성을 갖게 했다. 크리스퍼(CRISPR)라는 유전자 편집 기술을 이용했다. 높은 유전성을 감안할 때 유전자가 일단 이식되면 이론상 개체군 전체에 내성이 금방 퍼져나갈 것이라고 제임스 연구원은 말한다.
UC 어바인 연구팀은 얼룩날개 모기 유전체를 대상으로 연구를 실시했다. 인도 내 말라리아의 주요 매개체다. 매년 100만 명 이상의 환자가 발생해 500명 이상이 숨진다. 연구 결과는 지난 11월 23일 학술지 미국 국립과학원 회보에 실렸다. 그에 따르면 다른 종에도 그 기술이 통하리라 믿을 만한 이유가 있다. 연구에 참여하지 않은 메릴랜드대학 데이비드 오브록타 교수는 “말라리아 퇴치에 기여할 수 있는 시스템”이라고 평했다.
크리스퍼는 지난 2년 사이 유전자 변형 방식을 상당 부분 바꿔놓았다. 유전체 내 특정 부위의 DNA를 잘라 필요한 유전자를 삽입할 수 있도록 하는 방식이다. 기존의 방식에 비해 훨씬 빠르고 값이 싸다. UC 어바인 연구팀이 사용한 이 같은 말라리아 내성 삽입 기법은 예컨대 올해 초 초파리를 대상으로 처음 시연됐다. 연구팀은 불과 몇 개월 뒤 모기에 같은 방법을 적용하는 데 성공했다. 전통적인 유전자 편집 기술이었다면 다른 동물에 적용할 경우 미세 조정하는 데 더 오랜 시간이 걸렸을 것이다.
제임스 교수 연구팀이 이식한 2개의 유전자는 변형된 생쥐 면역 유전자다. 말라리아 원충에 달라붙어 숙주를 인식하지도, 모기의 체내에서 돌아다니지도 못하게 한다. 제임스 교수는 “장님이 됐다고 보면 된다”고 말했다. 결과적으로 그 기생충이 모기의 침샘 안으로 들어갈 수 없다. 따라서 모기가 물 때 사람 몸으로 옮겨 타지 못한다.
이 혁신기술을 현장에 적용하려면 약간의 수정이 필요하다고 제임스 교수는 말한다. 그리고 유전자 변형 생명체를 야생에 풀어놓으려면 말라리아가 유행하는 국가의 규제당국으로부터 승인을 받아야 한다. 그러나 앞으로 몇 년 뒤에는 가능하리라고 그는 기대한다.
크리스퍼 유전자 편집기법은 길지 않은 사용 기간 동안 다수의 윤리적 문제를 불러일으켰다. 지난 4월 과학자들이 그 기술을 이용해 인간 배아를 변형시켰다. 연구팀은 성장능력이 없는 배아를 이용해 말썽을 피하려 했지만 결국 논란의 소용돌이에 휘말리고 말았다. 현실세계에서 이 기술을 사용하기 전에 유전자 변형이 장기적으로 어떤 영향을 미칠지 더 많은 연구를 해야 한다고 제임스 교수는 말한다. 예컨대 ‘유전자 드라이브’가 다른 생명체로 확산될 될 경우 어떤 일이 일어날지 약간의 우려가 있다고 오브록타 교수는 밝혔다. 유전자 드라이브는 그런 특질이 거의 모든 자손에게 전달되도록 하는 유전적 메카니즘을 말한다. 어쩌면 바람직하지 않은 유전자가 개체 전체에 퍼져 한 종을 모두 멸종시킬지도 모른다. 그러나 그럴 가능성은 희박해 보이며 현재로선 말라리아 퇴치의 잠재적인 혜택이 더 크다고 제임스 교수는 말한다.
- DOUGLAS MAIN NEWSWEEK 기자 / 번역 차진우
ⓒ이코노미스트(https://economist.co.kr) '내일을 위한 경제뉴스 이코노미스트' 무단 전재 및 재배포 금지









![“오빠, 나 이러려고 만나?”... 한 번쯤은 공감했을 ‘그냥 필름’ [김지혜의 ★튜브]](https://image.isplus.com/data/isp/image/2026/03/03/isp20260303000042.400.0.jpg)
![“이 집에서 개가 제일 얌전”… 유튜브 ‘옥지네’가 보여주는 다정한 소란 [김지혜의 ★ 튜브]](https://image.isplus.com/data/isp/image/2026/02/22/isp20260222000072.400.0.jpg)



당신이 좋아할 만한 기사
브랜드 미디어
브랜드 미디어
[속보]다카이치, 호르무즈 함정 파견에 "트럼프에 日법률 설명"
세상을 올바르게,세상을 따뜻하게이데일리
이데일리
이데일리
“유모차 밀며 산책”…홍상수·김민희, 아들과 포착된 근황
대한민국 스포츠·연예의 살아있는 역사 일간스포츠일간스포츠
일간스포츠
일간스포츠
돌아온 BTS, 테일러 스위프트 뛰어넘나…전세계가 들썩
세상을 올바르게,세상을 따뜻하게이데일리
이데일리
이데일리
[마켓인]단기물에 2조 집행한 SK하이닉스…반도체 머니 시장 유입 본격화
성공 투자의 동반자마켓인
마켓인
마켓인
“인공눈물로 안 낫는다”…휴온스 ‘염증 종료’ 안구건조증 신약 도전
바이오 성공 투자, 1%를 위한 길라잡이팜이데일리
팜이데일리
팜이데일리