바이오
'유럽 승인' 셀트리온 코로나 치료제, 경쟁약물 대비 부작용 적어
- 렉키로나…발생가능한 부작용 ‘흔치 않은(uncommon)’ 수준의 알러지 반응 만 명시
로나프레베 다양한 부작용 명시, 베클루리 다수 알러지 반응 명시
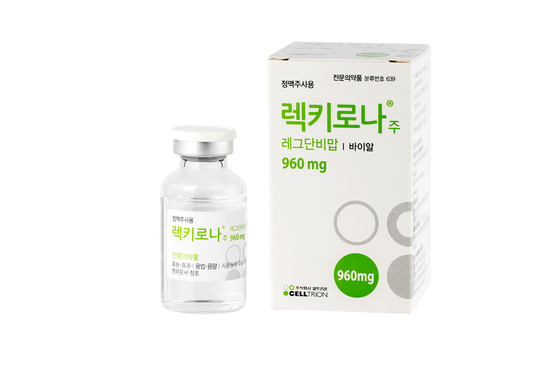
셀트리온이 개발한 코로나19 치료제 렉키로나는 지난 12일 EU의 판매 승인을 얻어 EU에서 승인된 3개의 코로나19 치료제 중 하나로 이름을 올린 바 있다. 길리어드사이언스의 베클루리는 앞서 승인받았으며, 리제네론 로나프레베는 렉키로나와 함께 승인됐다.
14일 유럽의약품청(EMA)에 공개된 렉키로나와 로나프레베, 베클루리의 의약품 설명서(packge leaflet)에 기재되는 부작용을 살펴본 결과 렉키로나가 가장 적은 수의 부작용이 보고된 것으로 나타났다.
렉키로나의 설명서에는 발생가능한 부작용으로 ‘흔치 않은(uncommon)’ 수준의 알러지 반응 만이 명시됐다. uncommon은 100명 중 1명 미만 영향을 미칠 수 있는 수준을 뜻한다. 반응으로는 발열, 호흡곤란, 심장박동 불규칙, 고혈압, 발진, 가려움증, 어지럼증 등이 명시됐다.
이에 반해 같은 날 승인받은 로나프레베의 경우 다양한 부작용이 명시됐다. 먼저 uncommon 항목으로 메스꺼움, 구역질, 어지러움, 발진 등이 명시됐고, 희귀한(Rare‧1000명 중 1명 미만) 수준으로 아나필락시스 등 심각한 알러지 반응 등이 명시됐다.
앞서 승인받은 베클루리의 경우 희귀 수준으로 주입 후 및 주입 중에 발생할 수 있는 다수의 알러지 반응이 명시됐다. 이 밖에 기타 부작용으로 매우 일반적인 수준(Very common‧10명 중 1명 이상)으로 간 효소의 증가 및 혈액 응고 지연, 일반적인 수준(common‧10명 중 1명 미만)에서 두통 등이 적혔다.
명시된 부작용이 적다고 해서 안정성이 높은 의약품이라고 단정하긴 어렵지만 환자들의 의약품 선택에 있어 긍정적인 영향을 예상할 수 있다.
특히 향후 경구용 치료제가 EMA에서 승인받더라도 이 약품들이 부작용에 대한 우려가 크다면 렉키로나를 선택할 이유는 충분하다. 미국 머크(MSD)의 몰누피라비르는 최근 영국 의약청(MHRA)에서 긴급승인을 받았는데, 약품의 설명서에는 common 수준의 설사‧구역질‧두통 등이, uncommon 수준으로 구토, 발진, 두드러기 등이 명시됐다. 몰누피라비르는 현재 EMA에선 ‘롤링리뷰’ 단계에 있다.
최윤신 기자
ⓒ이코노미스트(https://economist.co.kr) '내일을 위한 경제뉴스 이코노미스트' 무단 전재 및 재배포 금지









![면봉 개수 → 오겜2 참가자 세기.. 최도전, 정직해서 재밌다 [김지혜의 ★튜브]](https://image.isplus.com/data/isp/image/2025/12/21/isp20251221000019.400.0.jpg)
![갓 잡은 갈치를 입속에... 현대판 ‘나는 자연인이다’ 준아 [김지혜의 ★튜브]](https://image.isplus.com/data/isp/image/2025/11/21/isp20251121000010.400.0.jpg)


당신이 좋아할 만한 기사
브랜드 미디어
브랜드 미디어
주담대 7% 코앞…금융당국 ‘월별 관리’ 고삐 죈다
세상을 올바르게,세상을 따뜻하게이데일리
팜이데일리
일간스포츠
손담비, 신혼집 ‘월세 1000만 원’ 고백 "난리났다"
대한민국 스포츠·연예의 살아있는 역사 일간스포츠일간스포츠
일간스포츠
일간스포츠
"삼성전자 더 오른다"…분기 사상최대 실적에 증권가 목표가 잇단 상향
세상을 올바르게,세상을 따뜻하게이데일리
이데일리
이데일리
[마켓인]벼랑 끝 MBK…홈플러스 회생·고려아연 분쟁 ‘시계제로’
성공 투자의 동반자마켓인
마켓인
마켓인
라파스, 마이크로니들 비만패치 SC제형 반감기 넘었다..."기술 수출 기대 UP"
바이오 성공 투자, 1%를 위한 길라잡이팜이데일리
팜이데일리
팜이데일리